مواد فعال سطحی، شامل دو قسمت مجزاي ساختماني است، يك قسمت آبدوست (چربيگريز) و يك قسمت آبگريز (چربيدوست). هر چه زنجیر هیدروکربنی بلندتر باشد تمایل به جذب در سطح مشترک دو فاز بیشتر شده و در نتیجه کشش سطحی بیشتر کاهش مییابد و چون مواد فعال سطحی دارای سر آبدوست و آبگریز هستند حضور این دو گونه باعث پایداری لایههای سطحی و در نتیجه باعث پایداری سیستم میشود. هدف از این پژوهش تعیین چگونگی اندازهگیری مواد فعال سطحی است.
مواد فعال در سطح را به دلیل این که غلظت کمی از آنها در یک سیستم، انرژی آزاد سطح تماس بین فازهای موجود در آن را تغییر میدهد، عامل فعال سطحی نامیده میشود
یکی از مهمترین مواد صنعتی مورد مصرف ترکیبات فعال سطحی، سورفکتانتها هستند. سورفکتانتها مولکولهایی دو خصلتی بوده که دارای یک بخش قطبی و آب – دوست و یک زنجیره هیدروکربنی بلند غیرقطبی و آبگریز هستند
سورفکتانتها، عامل اصلی شویندگی در شویندهها هستند که از طریق سه فعالیت خیس کنندگی، معلق کنندگی و پراکنده ساختن باعث انجام فرایند شستشو میشوند.
اگر چه سورفکتانتها متنوع بوده ولی آنها در ایجاد پدیده خیس کنندگی عملکرد یکسانی دارند که با دارا بودن بخش قطبی و غیر قطبی و تناسب این دو بخش شدت یا تقلیل مییابد که این عملکرد و میزان آن با اندازهگیری تغییرات عاملی به نام کشش سطحی و یا بین سطحی ملموس میشود. لازم به توضیح است؛ کشش سطحی به کشش ایجاد شده بین یک مایع و هوا و کشش بین سطحی به کشش ایجاد شده میان یک مایع با مایع دیگر و یا یک جامد گفته میشود .
ویژگی های مواد فعال سطحی
مواد فعال سطحی، ويژگي بنيادي زير را دارا هستند:
- جذب سطحي: غلظت تعادلي يك ماده فعال سطحي در سطح تماس دو فاز بيشتر از غلظت آن در كل فضاي هر يك از فازهاست. به اين دليل است كه مقادير كم اين مواد ميتواند كشش سطحي را به مقدار زيادي كاهش دهند .
- خواص دو گانه آبدوستی و چربیدوستی: مولكول هر ماده فعال سطحي حاوي گروههاي داراي تمايل متضاد در انحلالپذيري است. يعني برخي گروهها به حل شدن در فاز قطبي متمايل هستند و گروههاي ديگر به انحلال در فازهاي غير قطبي تمايل دارند. اين ويژگي را با ضريب موازنه آب دوستی و چربي دوستی بيان ميكنند.
- انحلالپذيري: يك ماده فعال سطحي بايد حداقل در يكی از فازهای سیستم مایع محلول باشد تا بتوان آن را ماده فعال سطحي نامید.
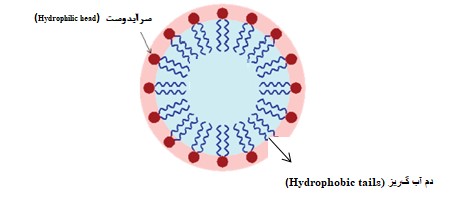
- توانايي تشكيل میسل: سورفکتانتها کشش سطحی آب را با جذب سطحی فصل مشترک هوا – آب کاهش میدهند؛ همچنین باعث کاهش کشش فصل مشترک آب و روغن با جذب سطحی فصل مشترک مایع- مایع میشوند. تعداد زیادی مولکول سورفکتانت میتوانند در توده محلول به هم وصل شده و تشکیل تودهای به نام میسلمیدهند. در واقع مولكولها يا يونهاي مواد فعال سطحي حل شده، وقتي كه غلظت آنها در محلول يك مايع به يك مقدار حداقل برسد، این انبوهههاي كوچك (میسل) را بهوجود ميآورند. به غلظتی که در آن این میسلها شروع به تشکیل شدن میکنند غلظت بحرانی تشکیل میسل میگویند. وقتی میسلها شروع به تشکیل شدن کردند دم آنها تشکیل یک هسته، مانند یک قطره روغن و سر یونی آنها یک پوسته بیرونی میسازد که تماس مطلوب با آب را بهبود میبخشد. در شکل زیر نمایی از تشکیل میسل ارائه شدهاست .
تصویری از نمای ساختار تشکیل میسل
- جهتگيري در سطح تماس دو مايع: مولكولها يا يونهاي فعال سطحي در سطح تماس دو فاز مايع و گاز لايه منظمي كه در آن ملكولها بهطور منظم جهتگيري كردهاند بهوجود ميآورند .
طبقهبندی مواد فعال سطحی
مواد فعال سطحی بهطور معمول با توجه به ماهیت گروههای آبدوست، به چهار گروه مواد فعال سطحی آنیونیک، کاتیونیک، غیریونی و آمفوتریک (یوندوقطبی) تقسیمبندی میشوند. این مواد دارای ویژگیهایی نظیر پاک کنندگی، پخش کنندگی و مرطوب کنندگی هستند. این مواد در صنایع مختلف از جمله کشاورزی، نساجی، داروسازی و محصولات بهداشتی کاربرد دارند .
مواد فعال سطحی آنیونیک:
مواد فعال سطحی آنيونيک دستهاي از مواد هستند كه هنگام حل شدن در آب توليد يك آنيون بزرگ ميكنند كه آنيون داراي گروه آبدوست و يك گروه چربي دوست است. این گروه از سورفکتانتها به دلیل قابلیت تمییز کنندگی بالا و تولید کف مناسب جزء سورفکتانتهای اصلی هستند. آنيونيکها ارزانترين گروه مواد فعال سطحی بوده و از نظر تجاري بيشترين فروش را دارا هستند .
مواد فعال سطحی کاتیونیک:
سورفکتانتهای کاتیونی در محلول آبی به یک کاتیون به نسبت بزرگ فعال و یک یون کوچک غیرفعال یونیزه میشود و دارای گروه آبدوست با بار مثبت هستند. ترکیبات کاتیونی علاوهبر اثرات امولسیونکننده و پاککننده، دارای فعالیت باکتریکش علیه باکتریهای گرم مثبت و گرم منفی هستند. بسیاری از ترکیبات ضدعفونی کننده معروف مانند بتادین و ستیل پیریدینیوم خواص سورفکتانتی دارند. این دسته بهطور معمول خاصیت شویندگی زیادی ندارند ولی در عوض هرگاه نیاز به نرمکنندگی، ضد الکتریسیته ساکن، دافع گرد و غبار، ضد باکتری و یا بازدارندگی خوردگی نیاز باشد میتوان از آنها استفاده کرد. مواد فعال سطحی کاتیونیک به علت داشتن قسمت آبدوست با بار مثبت روی بیشتر سطوح جامد جذب میشوند و میتوانند ویژگیهای خاص را به لایه انتقال دهند. این جذب، امکان تشکیل امولسیون در تماس با لایههای بار منفی را ایجاد میکند که منجر به رسوب فاز فعال در لایه میشود. همچنین با مواد فعال سطحی غیریونی و آمفوتریک سازگار هستند .
مواد فعال سطحی غیریونی:
ترکیبات فعال سطحی با بخش آبدوست بدون بار را ترکیبات فعال سطحی غیریونی مینامند. این مواد بهعنوان پاککننده بسیار مناسب بوده و به سختی آب حساس نیستند. این ترکیبات کاربرد گستردهای در ساخت مواد پاککننده دارند. مواد فعال سطحی غیریونی با انواع دیگر مواد فعال سطحی سازگار بوده و در برابر آب سخت، کاتیونهای فلزی چند ظرفیتی و الکترولیت در غلظت بالا مقاوم هستند. در آب و حلالهای آلی، شامل هیدروکربنها، قابل حل هستند. پلیاکسی اتیلن غیر یونی معمولا عامل پخشکننده بسیار عالی است .
مواد فعال سطحی آمفوتریک:
بار مواد فعال سطحی آمفوتریک توسط pH محلول کنترل میشود. به این معنا که در محیط قلیایی بهصورت مواد فعال سطحی آنیونی و در محیط اسیدی بهصورت مواد فعال سطحی کاتیونی عمل میکنند. این نوع از سورفکتانتها با انواع دیگر مواد فعال سطحی سازگار هستند. تحریکات کمتری برای پوست و چشم نسبت به انواع دیگر مواد فعال سطحی ایجاد میکنند و میتوانند روی سطوح با بار منفی یا مثبت بدون تشکیل لایه آبگریز جذب شوند.
مثالهایی از مواد فعال سطحی
- سدیم لوریل سولفات
- سدیم لوریل سولفات بهعنوان ماده فعال در سطح و کف کننده در خمیر دندان، شامپو و امولسیونهای محصولات آرایشی و بهداشتی مصرف میشود. بهطور معمول این ماده از سولفاته کردن الکلهای چرب (حاوی تعداد کربنهای زوج) که برش عمده آن لوریل است، بهدست میآید و فرمول آن CH3 (CH2)10CH2 OSO3 Na است.
شکل ظاهری: این ماده ممکن است به شکل پرک، پودر سوزنی، دانه دانه، بلور و یا مایع باشد. نمونه جامد ممکن است به رنگ سفید یا زرد روشن با بوی مخصوص به خود باشد. نمونه مایع در مایع 20 تا 30 درجه سلسیوس باید شفاف و عاری از هر گونه مواد خارجی باشد.
حلالیت: محلول 10 درصد سدیم لوریل سولفات در آب قابل حل، دارای خاصیت کف کنندگی، شفاف و در دمای 30 درجه سلسیوس میتواند کمی کدر باشد.
pH محلول یک درصد آن 5/9 – 5/7 است.
- سدیم لوریل اتر سولفات
سدیم لوریل اتر سولفات (SLES) با نام تجاری تگزاپون یک ماده شیمیایی خمیر شکل، نیمه شفاف به رنگ سفید یا مایل به زرد است. تگزاپون در دسته مواد فعال سطحی آنیونی قرار دارد و از خانواده آلکیل اتر سولفاتها است. این ماده حاصل ترکیب یک الکل چرب مانند روغن نارگیل با اکسید اتیلن و متعاقب آن سولفوناسیون است. تگزاپون بوی ملایمی دارد و شرکتهای تولیدکننده، آن را در غلظتهای ۳۰ و ۷۰ درصد تولید و عرضه میکنند .این ماده حاوی مقدار اندکی نمک است؛ هنگام رقیق شدن با آب در غلظتهای معمولی ویسکوزیته پایینی از خود نشان میدهد و با افزودن سدیم کلراید و آلکانول آمید به آن، ویسکوزیتهاش تنظیم میشود.
شکل ظاهری سدیم لوریل سولفات با توجه به درجهبندی آن در دمای °c25 بهصورت خمیر تقریبا شفاف و یا بهصورت شفاف بیرنگ تا زرد کهربایی و مایعی گرانروا است .
پایداری: سدیم لوریل اتر سولفات باید در دمای حدود 25 درجه سلسیوس هیچ گونه تغییر فیزیکی و شیمیایی نداشته باشد [4]. pH محلول 5 درصد، با توجه به نوع درجهبندی آن 7 – 9 است .
- سید سولفونیک (آلکیل بنزن سولفونیک اسید)
اسید سولفونیک یا آلکیل بنزن سولفونیک اسید که به اختصار آن را LABSA مینامند، نوعی سورفکتانت آنیونی بهصورت مایع ویسکوز قهوهای رنگ است. همانطور که از نام این ماده پیداست، این ماده خاصیت اسیدی داشته و خورنده است و باید در مخازن استیل نگهداری شود. ماده اولیه اسید سولفونیک، آلکیل بنزن خطی است. سپس آلکیل بنزن خطی همچون تگزاپن در کارخانههای سولفوناسیون، سولفونه شده و به اسید سولفونیک تبدیل میشود.
اسید سولفونیک سورفکتانت آنیونی با قدرت شویندگی و سازگاری با دامنه وسیعی از سورفکتانت های آنیونی، کاتیونی و آمفوتری دیگر است. این محصول سورفکتانت حد واسط بسیار کارآمدی است که معمولا با انواع قلیاها خنثی شده و سولفوناتها را تشکیل میدهد که در زمینههای مختلفی مورد استفاده است. این محصول قابلیت استفاده در محیطهای اسیدی را دارا است. اين ماده يكي از ارزانترين، مهمترین و پر مصرفترین سورفكتانتهاي مصرفي در صنايع شويندههای پودری و مایع است.
فرمول عمومی این اسید HSO3R که R میتواند متان یا بنزن و غیره باشد. اسید سولفونیک محلول در آب، غیر فرار و جاذب رطوبت است که بهعنوان عوامل امولسیون کننده، مواد افزودنی و روغنهای روان کننده مورد استفاده قرار میگیرد.
از ویژگیهای ظاهری این اسید میتوان به ویسکوزیته بسیار بالای آن اشاره نمود که تقریباً مانند عسل ویسکوز است. رنگ آن از قهوهای روشن تا قهوهای تیره تغییر میکند.
شکل ظاهری: سولفونیک اسید باید بهصورت مایع همگن، عاری از ذرات معلق و به رنگ قهوهای روشن باشد .
حلالیت: این اسید در آب و الکل حل میشود، اما در حلالهای غیرقطبی، نامحلول است.
دانسیته: 1/32گرم بر سانتیمتر مکعب.
تشخیص سریع مواد تانسیواکتیو
مواد آلی فعال در سطح، چنانچه با آب به غلظت 5/0 درصد در دمای °C20، مخلوط شوند به مدت یک ساعت در همان دما بهصورت ثابت قرار گیرند:(الف): مایعی شفاف یا نیمه شفاف یا یک امولسیون پایدار بدون تفکیک ماده انحلالپذیر ایجاد میکنند[10].
(ب): کشش سطحی آب را به N/m 2-10×5/4 یا کمتر کاهش میدهند [10].
تعیین میزان ماده آنیونی
- محلول ذخیره شناساگر مخلوط:
g 005/0 ± g 5/0 از دیمدیوم بروماید را در یک بشر وزن کنید. g 005/0 ± g 25/0 دی سولفین بلو را در یک بشر دیگر وزن کنید. ml 25 تا ml 30 از محلول داغ اتانول – آب ( V/V) 10 به1 به هر یک از بشرها اضافه کنید. محلولها را هم بزنید تا رنگها حل شوند. سپس هر دو محلول را در یک بالن ml 250 به حجم برسانید. این محلول به مدت 6 ماه قابل نگهداری است[1].
- محلول شناساگر اسیدی:
ml 200 آب و ml 20 از محلول شناساگر ذخیره مخلوط را به یک بالن حجمی ml 500 در سمبادهای بریزید. ml 20 از اسید سولفریک mol/l 5/2 به آن افزوده و خوب مخلوط کرده و به حجم برسانید. این محلول را در تاریکی نگهداری کنید
روش آزمون
ابتدا نمونه یک درصد تهیه کنید. چند قطره فنول فتالئین اضافه کنید و با محلول سدیم هیدروکسید mol/l 1 و یا درصورت نیاز با اسید سولفوریک mol/l 5/0 تا رسیدن به رنگ صورتی کم رنگ، خنثی کنید. سپس 20 سیسی از محلول را در یک استوانه مدرج در سمبادهای ریخته، ml 10 آب، ml 15 کلروفرم و ml 10 شناساگر اسیدی به آن اضافه کنید. مقدار کمتر از یک اکیوالان از بنزوآلکونیوم کلراید اضافه کنید و برای 30 ثانیه به شدت ظرف را تکان دهید. تا شکستن امولسیون و ظاهر شدن دو فاز، استوانه را در حال سکون قرار دهید. لایه پایینی در ابتدا صورتی خواهد بود. تیتراسیون را ادامه دهید و بعد از هر افزایش تیتر کننده حداقل 15 ثانیه ظرف را به شدت تکان دهید. به هنگام رسیدن به نقطه پایانی، امولسیون تشکیل شده به آسانی شکسته میشود. تیتراسیون را با افزودن قطرات تیتر کننده و تکان دادن ما بین هر افزایش ادامه دهید تا به نقطه پایانی برسد. هنگامی که رنگ صورتی کاملاً از لایه کلروفرم محو شد و رنگ آبی خاکستری کم رنگ ایجاد شد، بهعنوان نقطه پایانی در نظر بگیرید. حجم تیتر کننده اضافه شده را یادداشت کنید. درصد جزء فعال آنیونی را از معادله زیر محاسبه کنید:
حجم محلول بنزآلکونیوم کلراید بر حسب میلی لیتر V
غلظت محلول بنزآلکونیوم کلراید بر حسب N
اکی والان گرم ماده فعال آنیونی Ew
حجم محلول برداشتی برحسب میلی لیترD
V حجم بالن رقیق سازی بر حسب میلی لیتر
جرم نمونه برداشتی برحسب گرم m
تعیین میزان ماده کاتیونی
- روش آزمون:
نمونه آزمون (آزمونه) نمونه آزمايشگاهي كه داراي 002/0 يا 004/0 مول ماده فعال كاتيوني باشد را با دقت يك ميليگرم وزن كنيد.
يادآوري: حجم تيتراسيون بين 10 تا 20 ميليليتر ميشود.
آزمونه را در 20 ميليليتر ايزوپروپانل حل كنيد؛ درصورت لزوم آن را گرم نموده و حدود 50 ميليليتر آب افزوده و هم بزنيد. آن را به بالن ژوژه 1000 ميليليتري منتقل كرده و با آب تا خط نشانه به حجم برسانيد. اين محلول را A بناميد. با استفاده از پيپت، 10 ميليليتر از محلول استاندارد سديم لوريل سولفات 004/0 مول در ليتر را به مرور وارد كرده و 10 ميليليتر آب و 15 ميليليتر كلروفورم و 10 ميلیليتر محلول شناساگر مخلوط را اضافه كنيد. بورت بند را با محلول آزمون A پر كنيد. محلول سديم لوريل سولفات را با محلول آزمون A تيتر كنيد، در مزور را بسته پس از هر افزايش خوب تكان دهيد.
لايه پاييني كلروفرمی داراي رنگ صورتي است. در مرحله رسيدن به نقطه انتهايي، فرم امولسيوني تشكيل شده سريع شكسته شده و رنگ لايه كلروفرمي كمرنگ ميشود. از اين مرحله، تيتراسيون را قطره قطره ادامه داده و پس از هر افزايش مزور را كاملا تكان دهيد تا نقطه انتهايي بدست آيد. در اين لحظه رنگ صورتي بهطور كامل در لايه كلروفرمي از بين رفته و به رنگ آبي خاكستري كمرنگ تبديل ميشود و با افزايش بيشتر محلول A، لايه كلروفرمي تبديل به آبي ميشود؛ حجم محلول A مورد نياز براي تيتراسيون را يادداشت كنيد [2].
مقدار ماده فعال كاتيوني بر حسب درصد وزني از رابطه زير بهدست ميآيد:
که در آن:
(C) غلظت واقعي C12H25NaSo4 از محلول سديم لوريل سولفات بر حسب مول در ليتر
Mr وزن ملكول نسبي ماده فعال كاتيوني
(V) حجم محلول
A مصرفي براي تيتراسيون بر حسب ميلیليتر
(m) وزن آزمونه بر حسب گرم است.
نتیجهگیری
مواد فعال سطحی با دارا بودن بخشهای قطبی و غیرقطبی و قرار گرفتن بین مولکولهای سطحی باعث میشوند که سطح تماس بین مایع با هوا یا چیز دیگر کاهش یابد؛ به عبارتی، مواد فعال سطحي به دلیل ويژگي ساختاري خود ميتوانند كشش سطحي آب را كاهش دهند. با كاهش كشش سطحي، سطح تماس افزايش مييابد و موجب ویژگیهایی مانند پاك كنندگي، ويسكوز دهندگي، امولسيون کنندگی، كف كنندگي و غيره ميشوند. مواد فعال سطحي كاربردهاي فراواني در صنايع مختلف نظير صنت نفت و گاز، كشاورزي، صنايع غذايي، داروسازي و غيره دارند.












